Profesión
aliciaserrano
Dom, 23/08/2020 - 07:00
Oportunidad de negocio

El preservativo  es un artÃculo que parece que se le está escapando de las manos a la farmacia y que, sin embargo, está creciendo en grandes superficies.
Salud sexual es una categorÃa que todavÃa tiene poco recorrido en botica, aunque está cobrando cada vez más fuerza de la mano de un completo consejo profesional,
De hecho, “el margen de esta categorÃa, bien gestionada, es del 35-40% aproximadamente, en función de las negociaciones que se hagan con los laboratoriosâ€, calcula Silvia Fortuny, gerente y fundadora de Fortuny&Consultores. Â
Añade que tiene un gran potencial, “puesto que todos los clientes de la farmacia, en mayor o menor o menor medida, tienen o practican sexo; y si no lo hacen, desde el consejo farmacéutico podemos informar y aclarar situaciones o anomalÃas que ayuden a dichos clientes a vivir su sexualidad de forma plenaâ€, dice.
El sexo es salud, y la salud incluye sexo
Es posible utilizar otros nombres para abordar esta categorÃa, como salud Ãntima o sexo saludable, “de forma que el cliente de la farmacia no solo la relaciones con patologÃa, sino con saludâ€, indica Fortuny.
Además, puede abordarse desde las diferentes etapas de la mujer y el hombre (niñez y adolescencia, etapa fértil y menopausia), y cada una de ellas con productos y servicios asociados.
“Incluye desde higiene Ãntima, bolas para el suelo pélvico, copas menstruales, preservativos (existen preservativos para veganos), geles lubricantes, estimuladores, suplementación nutricional relacionada con el deseo sexual… incluso se pueden colocar test de embarazo en el linealâ€, asegura.
La higiene Ãntima y los complementos nutricionales son los más demandados
Los productos que ayudan a una vida sexual saludable son imprescindibles para que esta categorÃa esté bien trabajada, como lubricantes, complementos nutricionales, higiene Ãntima, material tipo flyers con información de interés, métodos anticonceptivos…
“La higiene Ãntima y los complementos nutricionales son los que tienen más potenciaâ€, dice MarÃa Palop, titular de Farmacia Boix.
Palop también es fundadora Boix Cosmetics y Biomimetic Cosmetics PBT y lleva años gestionando la categorÃa de salud sexual en su botica. “La farmacia es uno de los principales puntos de salud para el paciente por lo que es importante trasmitir este tipo de mensajes relacionados con la salud sexualâ€, añade Palop.Â
El valor del consejo y zona Ãntima
La diferenciación de la farmacia frente a las grandes superficies es precisamente el consejo. “Hay que saber hacer preguntas sutiles y bien orientadas, con mucha empatÃa y con una gran formación, para averiguar qué le preocupa al cliente, cuál es su situación, si le apetece hablar del tema… Hay que hacerle llegar que la farmacia es un excelente punto de informaciónâ€, recomienda Fortuny.
En Farmacia Boix disponen de un espacio personalizado para atender este tipo de cuestiones, aunque dice que cada vez hay más gente a la que no le resulta incómodo hablar de estos temas.
“Esta categorÃa tiene un peso importante en la botica, pues de ella depende la rotación de productos de muchas otras categorÃas de la farmacia tales como la higiene Ãntima, los preservativos e incluso la complementación nutricionalâ€, dice.
Un mensaje claro y directo
Palop añade que gestionar una categorÃa de este tipo no es complicado, pero dice que es importante saber qué mensaje se quiere transmitir.

Campaña sobre Salud sexual en Farmacia Boix (Valencia).
“Querer hacer una campaña de salud sexual puede resultar muy atractivo, pero necesitamos un mensaje claro y directo para conseguir captar la atención de la gente. La salud sexual abarca muchos temas, por lo que es importante escoger lo que creemos que puede funcionar mejor para nuestra farmaciaâ€, recomienda.
Recuerda que hacer una campaña de estas caracterÃsticas hace que se activen muchas categorÃas y que, a la vez que se da un mensaje claro y directo, también es importante exponer productos especÃficos y relacionados con dicho mensaje. “Hay que ligarlo todoâ€, indica.
MÃnimo 6 lineales
La categorÃa debe ubicarse en una zona Ãntima de la farmacia, donde se pueda mirar con calma, tocar, oler o incluso probar texturas a través de tester, “siempre bajo la mirada atenta del personal, que debe estar pendiente del momento en el que esa persona puede necesitar ayudaâ€, dice Palop.Â
El producto de esta categorÃa es tan extenso y variado que “da para tener un lineal completo de 6 estanterÃas, como mÃnimoâ€, añade Fortuny.
También aclara que ello debe decidirse en función de la estrategia de la oficina de farmacia: “Incluso se pueden tener dos marcas por subcategorÃa, conociendo las ventajas de cada una de ellas y el valor añadido que ofrecenâ€.Â
En opinión de Palop lo mejor también es tener un par de marcas de calidad y trabajar el vademécum prácticamente en su totalidad. “A dÃa de hoy existen muchas marcas para el cuidado Ãntimo y que están relacionadas con una salud sexual saludable, y todas ofrecen infinidad de productosâ€.
El preservativo es difÃcil de rentabilizar
El preservativo  es un artÃculo que parece que se le está escapando de las manos a la farmacia y que, sin embargo, está creciendo en grandes superficies. “Probablemente esto se debe a que los factores intimidad y comodidad hacen más propicio ese canal para comprar, ya que no se pasa vergüenza en la venta de autoservicio, los precios y promociones son buenas y nadie pregunta si se prefiere un gel sabor chocolate, fresa o mangoâ€, asegura Fortuny.
El preservativo es, según la titular de Farmacia Boix, uno de los artÃculos más difÃciles de rentabilizar y con los que no deberÃa desgastarse mucho la farmacia.
“Existe una guerra de precios con las grandes superficies y es muy difÃcil competir. Hay que buscar artÃculos y sobre todo laboratorios que den el apoyo necesario que necesita la farmaciaâ€, aconseja Palop.Â
Hay productos como las bolas de suelo pélvico y los ejercitadores que pueden tener doble y triple implantación, “es decir, que pueden estar expuestos en otras categorÃas como Selenials, Menopausia o Maternidadâ€.Â
También existen tampones y compresas ecológicas, biodegradables y compostables. “Otra categorÃa al alzaâ€, indica Fortuny.Â
Cómo colocar la categorÃa
Al igual que cuando trabajamos cualquier otra campaña, el producto tiene que estar visible y bien señalizado.
“A la altura de los ojos deberemos colocar aquellos artÃculos más especÃficos: hidratantes vulvares, lubricantes, probióticos vaginales y sobre todo aquellos que resulten más novedosos. Por encima de los mismos colocaremos productos de higiene Ãntima tales como geles, toallitas, sprays…Y por debajo todos aquellos que respondan a la vÃa oral tales como los complementos nutricionales que ayudan a mantener una vida sexual saludableâ€, recomienda Palop.Â
En su opinión, se deberÃa dedicar un espacio con visibilidad suficiente y que ayude a reconocer esta categorÃa. “Dependerá del espacio que tengas, pero recomiendo alrededor de unos 5 lineales aproximadamente", añade.
Competir con otros canales
La gente está acostumbrada a ir a comprar a la farmacia cuando tiene un problema. Y ocurre lo mismo con los productos OTC.
“Por suerte, cada vez más se reconoce a la farmacia como un espacio de salud en el que se pueden encontrar infinidad de productos para el cuidado diario y la prevención. Por supuesto que hay que competir con el resto de canales, principalmente por el precio. La farmacia no tiene la misma capacidad de compra que una gran superficie, pero el consejo y la especialización tienen que ser el factor clave para que el consumidor acabe comprando en la farmaciaâ€, señala Palop.
Promociones y campañas
Para Palop, las promociones siempre son un valor añadido, pero no se puede pretender que una categorÃa solo funcione asÃ.
“Lo importante es trabajar muy bien el producto, dar un buen consejo y ayudarnos de algunas muestras que nos puedan proporcionar los laboratorios para dar a conocerlo. Lo ideal, en mi opinión, serÃa hacer una promoción unas tres veces al año para esta categorÃa, aunque dependerá  mucho del tipo de farmacia y de la demanda que se tengaâ€.
También se puede ayudar con algunos talleres con temas que sean de interés para hablar de una vida sexual saludable, “e incluso participar con algunos colegios para ayudarles a resolver todas aquellas dudas que les inquietanâ€, añade Palop.
Especializados en menopausia
Teresa Bonnin, titular de Farmacia Bonnin (Palma de Mallorca), lleva más de 5 años gestionando la categorÃa Menopausia, que es una parte de Salud Sexual.Â
De hecho, en la farmacia hay dos zonas ZAP. La primera está en la oficina donde se realiza la primera entrevista ante una consulta sobre una dispensación o indicación farmacéutica, con un sencillo cuestionario de menopausia de 6 preguntas rápidas conocido como The Menopause Quick 6 questionnaire (MQ6), que no se tarda más de 2 minutos en realizarlo.

sofocos
“Según vemos la percepción en la calidad de vida que tiene la mujer, citamos a una segunda ZAP para una consulta de una hora protocolizada, en la que realizamos una historia clÃnica y nutricional y le realizamos la Escala Cervantes, para evaluar su calidad de vidaâ€, dice Bonnin.
Si se compara esta categorÃa con Ãntima “puede tener un peso de un 80%, aunque deberÃa compararse con otras, ya que también puede incluir complementos nutricionales, medicamentos de indicación farmacéutica, categorÃa sueño, productos sanitarios, fitoterapia, salud sexual, dermofarmacia, capilar...Â
Los lubricantes e hidratantes internos y externos, y la fitoterapia para los sofocos son algunos de los productos estrella
Para trabajar bien esta categorÃa, Bonnin recomienda contar con productos de higiene intima, lubricantes e hidratantes internos y externos, óvulos vaginales, cremas intimas antiedad, aceites de masaje, ayudas de fisioterapia para suelo pélvico, fitoterapia para sofocos con evidencia, complementos nutricionales para insomnio e irritabilidad, deseo sexual hipoactivo, prevención osteoporosis, omega 3, antioxidantes, salud digestiva, sÃndrome metabólico, colágenos y probióticos.
“Para ello debemos disponer de referencias claves, que en muchos casos se demanden por prescripción médica, y estar formados en medicamentos: terapia hormonal, osteoporosis, onocologÃa y otras que puedan satisfacer las necesidades de nuestro público, como ejercitadores de suelo pélvico, constituyendo un posicionamiento estratégico en la categorÃa y permitiendo obtener beneficios que rentabilicen la inversión de nuevos productosâ€.
El espacio, según Bonnin, debe ocupar un lineal de 4-5 baldas, y en precios considera que debe tener un margen alrededor del 30%. “Hay que buscar laboratorios que nos den buenas condiciones de compra, formación y que nos ayuden a desarrollar esta categorÃaâ€.
Los artÃculos más difÃciles de rentabilizar son los de fisioterapia de suelo pélvico y deseo sexual
Los productos de fisioterapia de suelo pélvico y deseo sexual son los más difÃciles de rentabilizar, “aunque se podrÃan generar acciones orientadas a fomentar la indicación de estos productos con charlas y con otros profesionales como fisioterapeutas, ginecólogos y sexólogosâ€.
No obstante, los productos que tiene más potencial son los complementos en insomnio e irritabilidad, hidratantes y lubricantes vaginales, y complementos nutricionales con indicación en la prevención de un envejecimiento saludable.
Se puede abordar desde las distintas etapas de la mujer y del hombre. Bien gestionada, además, puede dejar un margen del 40% en la farmacia.
Off
Alicia Serrano
Off
 Los pacientes anticoagulados reclaman sistemas de autocontrol o flexibilización de los visados durante la epidemia de coronavirus.
Los pacientes anticoagulados reclaman sistemas de autocontrol o flexibilización de los visados durante la epidemia de coronavirus.
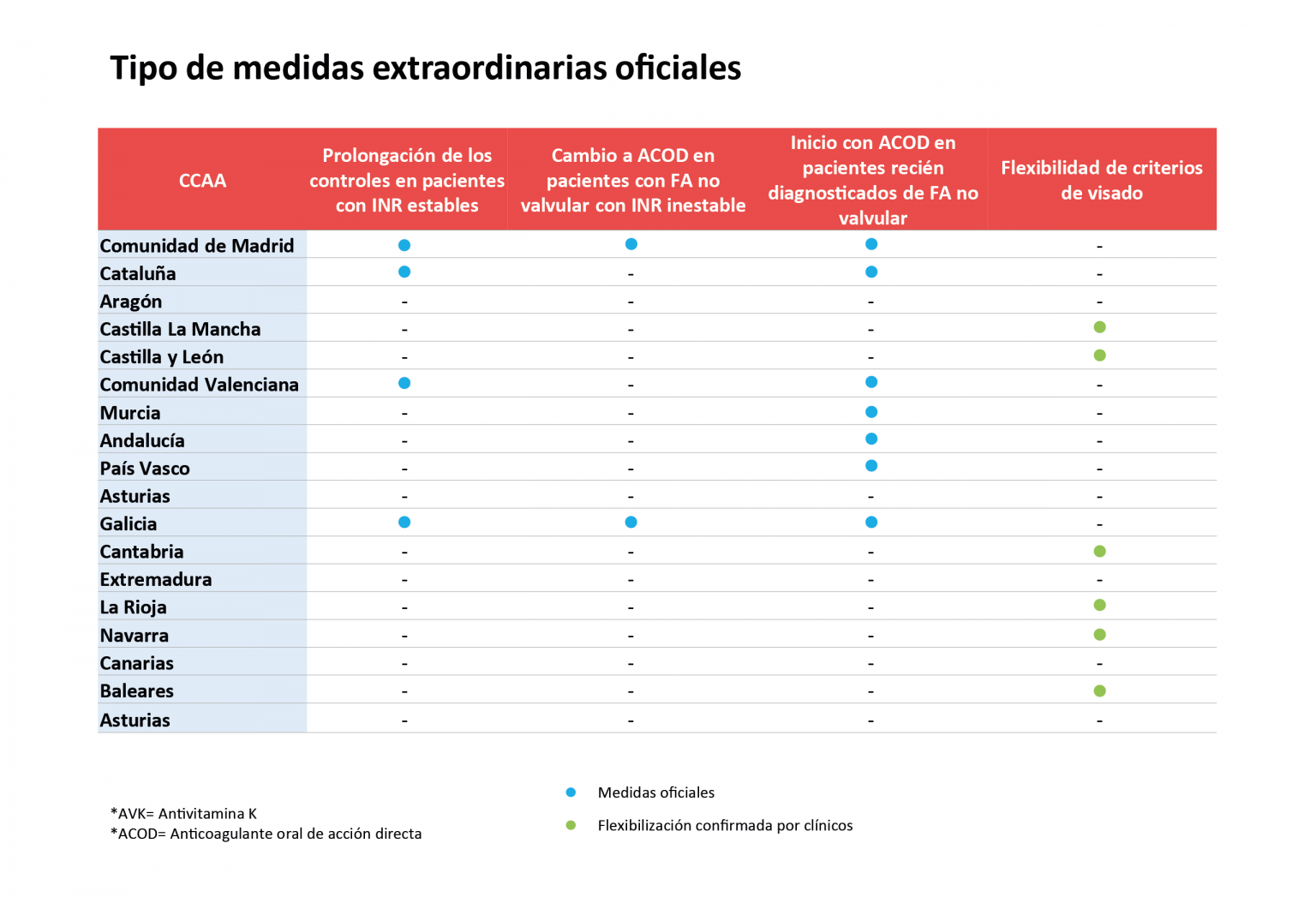 Medidas adoptadas por las autonomÃas para flexibilizar el acceso a anticoagulación durante la pandemia de coronavirus. (Fuente: Feasan)
Sólo 7 autonomÃas flexibilizaron las medidas en el pico de la pandemia
Medidas adoptadas por las autonomÃas para flexibilizar el acceso a anticoagulación durante la pandemia de coronavirus. (Fuente: Feasan)
Sólo 7 autonomÃas flexibilizaron las medidas en el pico de la pandemia


 La nueva app de Nestlé Health Science pretende formar una comunidad en la que los profesionales puedan formarse.
La nueva app de Nestlé Health Science pretende formar una comunidad en la que los profesionales puedan formarse.
 La plataforma 'We Are Nutrition' ofrece herramientas para el diagnóstico y realidad aumentada.
La plataforma 'We Are Nutrition' ofrece herramientas para el diagnóstico y realidad aumentada.
 El teletrabajo es totalmente voluntario y no hay una norma especÃfica en España que lo regule.
El teletrabajo es totalmente voluntario y no hay una norma especÃfica en España que lo regule.
 España continúa siendo el segundo paÃs europeo con más contagios desde el inicio de la pandemia (439.286), solo por detrás de Rusia (975.576).
España continúa siendo el segundo paÃs europeo con más contagios desde el inicio de la pandemia (439.286), solo por detrás de Rusia (975.576).







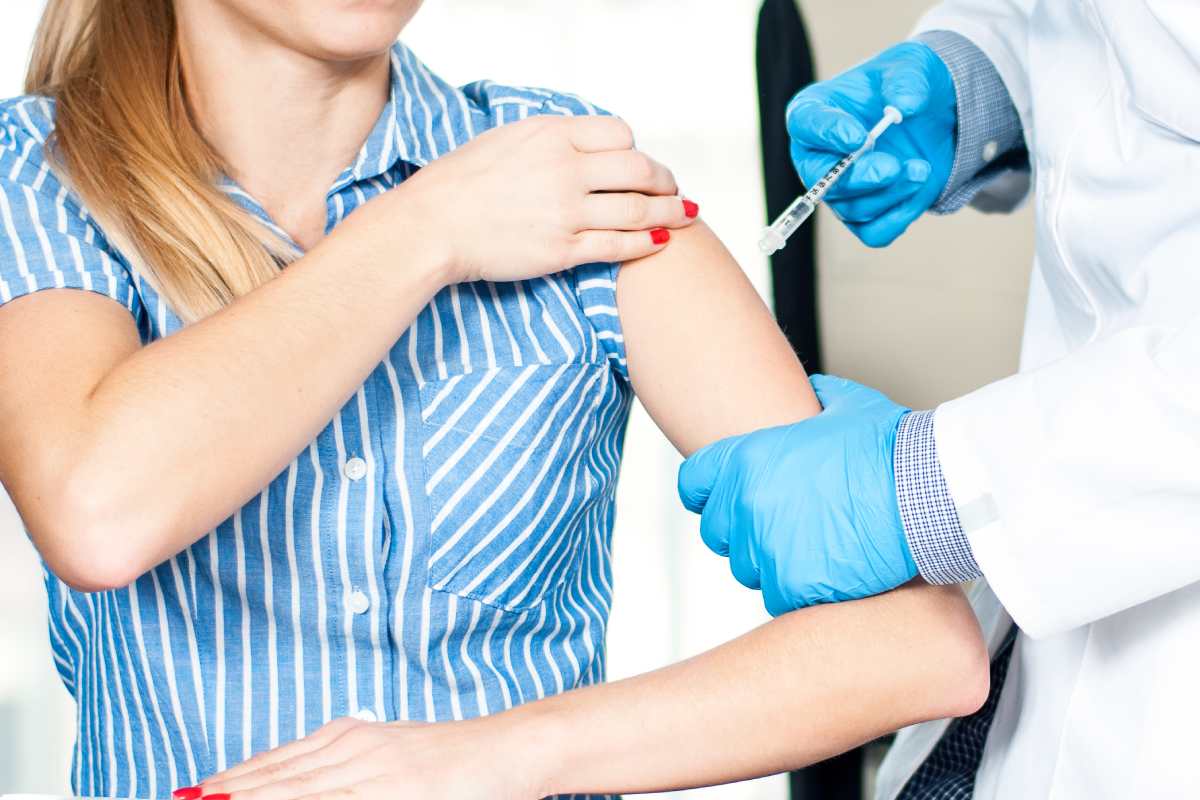 La vacuna se administrará en 10 grupos de tratamiento en función de la edad, con edades comprendidas entre los 18 y 55 años, y en mayores de 65.
La vacuna se administrará en 10 grupos de tratamiento en función de la edad, con edades comprendidas entre los 18 y 55 años, y en mayores de 65.
 Manuel Cascos, presidente de Satse, en el Congreso de los Diputados.
Manuel Cascos, presidente de Satse, en el Congreso de los Diputados.
 Aceese recomienda la incorporación de la enfermera escolar en todos los centros que no dispongan de esta figura antes del inicio del curso escolar, con el fin de preparar los espacios, gestionar el contacto con los padres, realizar educación preventiva, detectar signos y sÃntomas del virus, derivar a los centros de primaria, y realizar el rastreo y seguimiento de los casos positivos. FOTO: Aridna Creus y Ãngel GarcÃa (Banc Imatges Infermeres).
Aceese recomienda la incorporación de la enfermera escolar en todos los centros que no dispongan de esta figura antes del inicio del curso escolar, con el fin de preparar los espacios, gestionar el contacto con los padres, realizar educación preventiva, detectar signos y sÃntomas del virus, derivar a los centros de primaria, y realizar el rastreo y seguimiento de los casos positivos. FOTO: Aridna Creus y Ãngel GarcÃa (Banc Imatges Infermeres).
 Engrà cia Soler Pardo, presidenta de la Asociación CientÃfica Española de EnfermerÃa y Salud Escolar (Aceese) y la Asociación Catalana de EnfermerÃa y Salud Escolar (Acise).
Engrà cia Soler Pardo, presidenta de la Asociación CientÃfica Española de EnfermerÃa y Salud Escolar (Aceese) y la Asociación Catalana de EnfermerÃa y Salud Escolar (Acise).
 Salvador Illa, ministro de Sanidad.
Salvador Illa, ministro de Sanidad.
 Hal Barron, director cientÃfico y presidente de I+D de GSK.
Hal Barron, director cientÃfico y presidente de I+D de GSK.
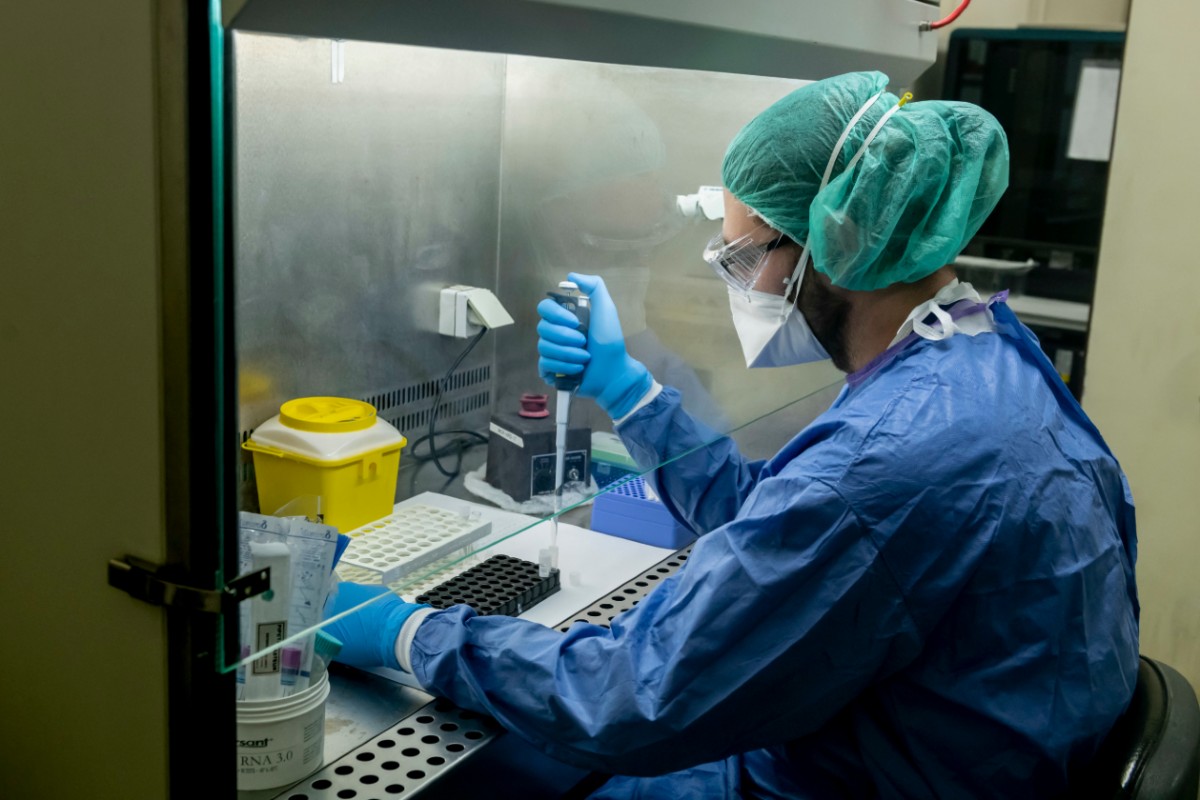 En un mes, el número de PCR realizadas en una semana ha aumentado un 76% (Foto: José Luis Pindado)
En un mes, el número de PCR realizadas en una semana ha aumentado un 76% (Foto: José Luis Pindado)
 Caballerizas Reales de la Magdalena, sede del VIII Curso de Traducción Médica UIMP Santander.
Caballerizas Reales de la Magdalena, sede del VIII Curso de Traducción Médica UIMP Santander.

 Alberto Borobia, coordinador de la Unidad Central de Investigación ClÃnica y Ensayos ClÃnicos de La Paz.
Alberto Borobia, coordinador de la Unidad Central de Investigación ClÃnica y Ensayos ClÃnicos de La Paz.
 Alberto Borobia junto al equipo de la Unidad de Ensayos de La Paz.
Alberto Borobia junto al equipo de la Unidad de Ensayos de La Paz.


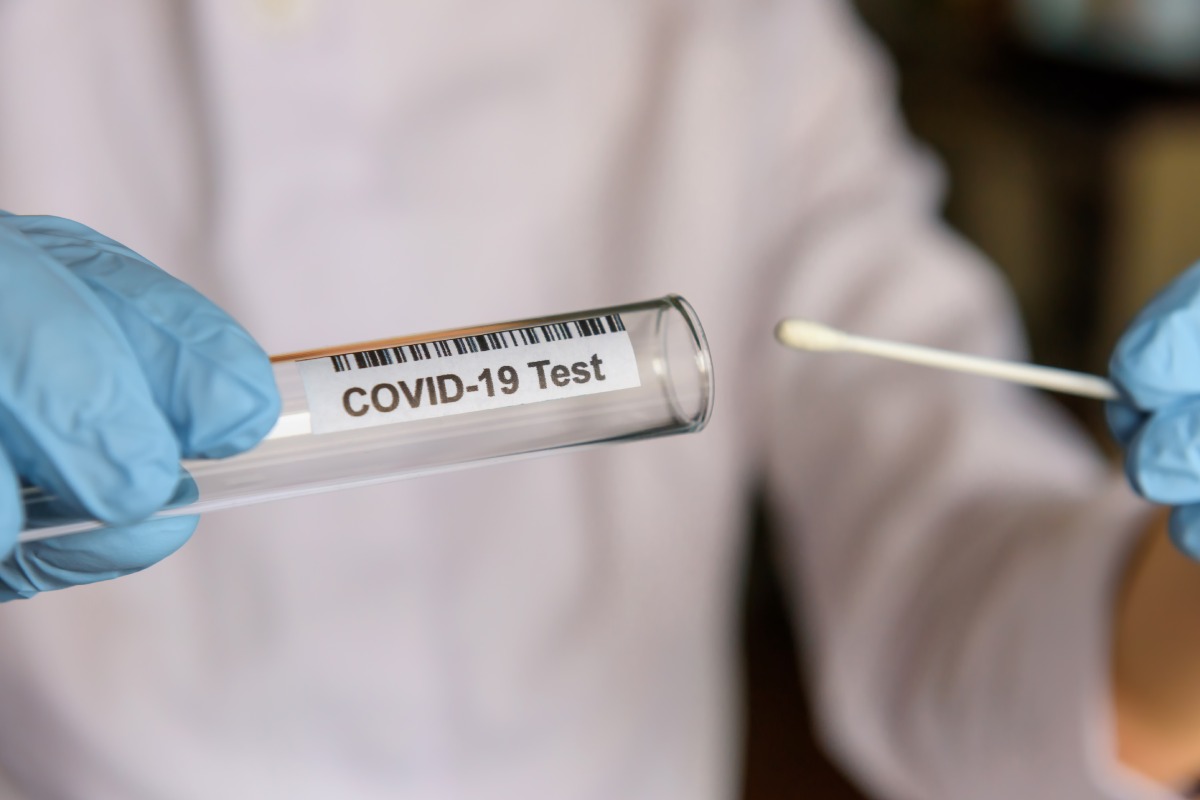



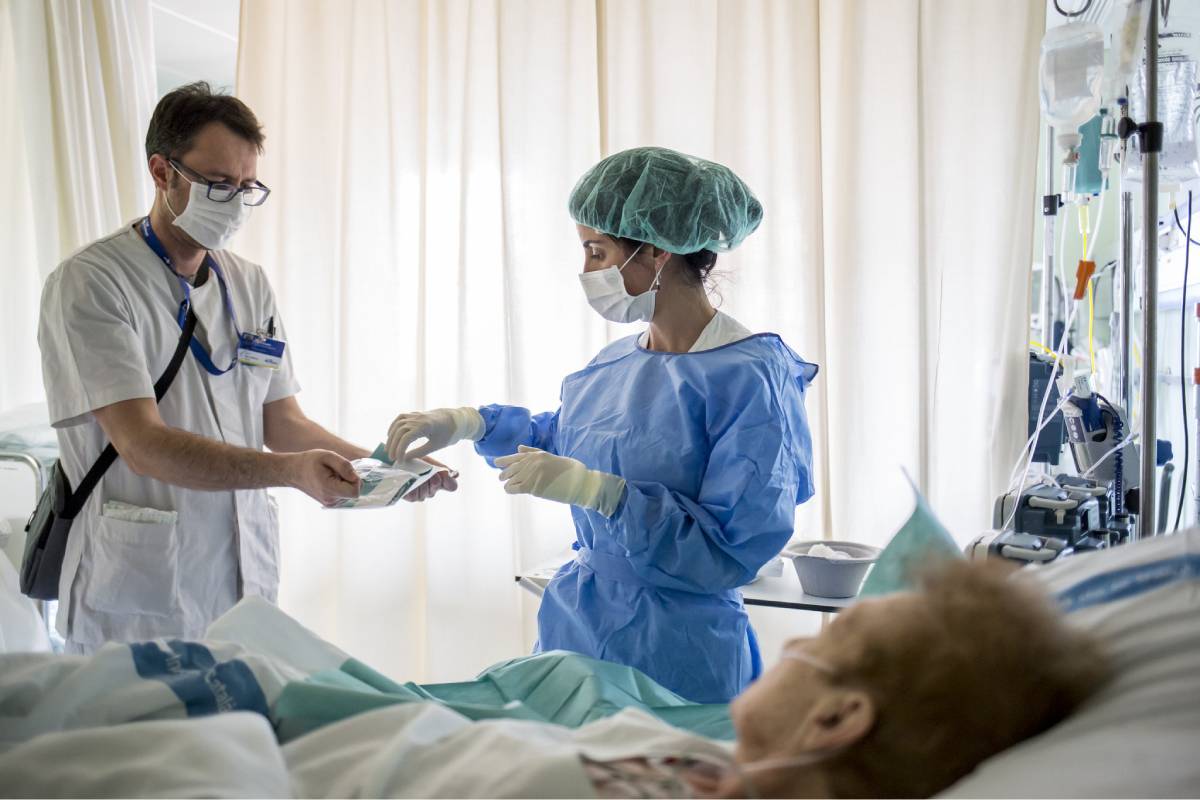
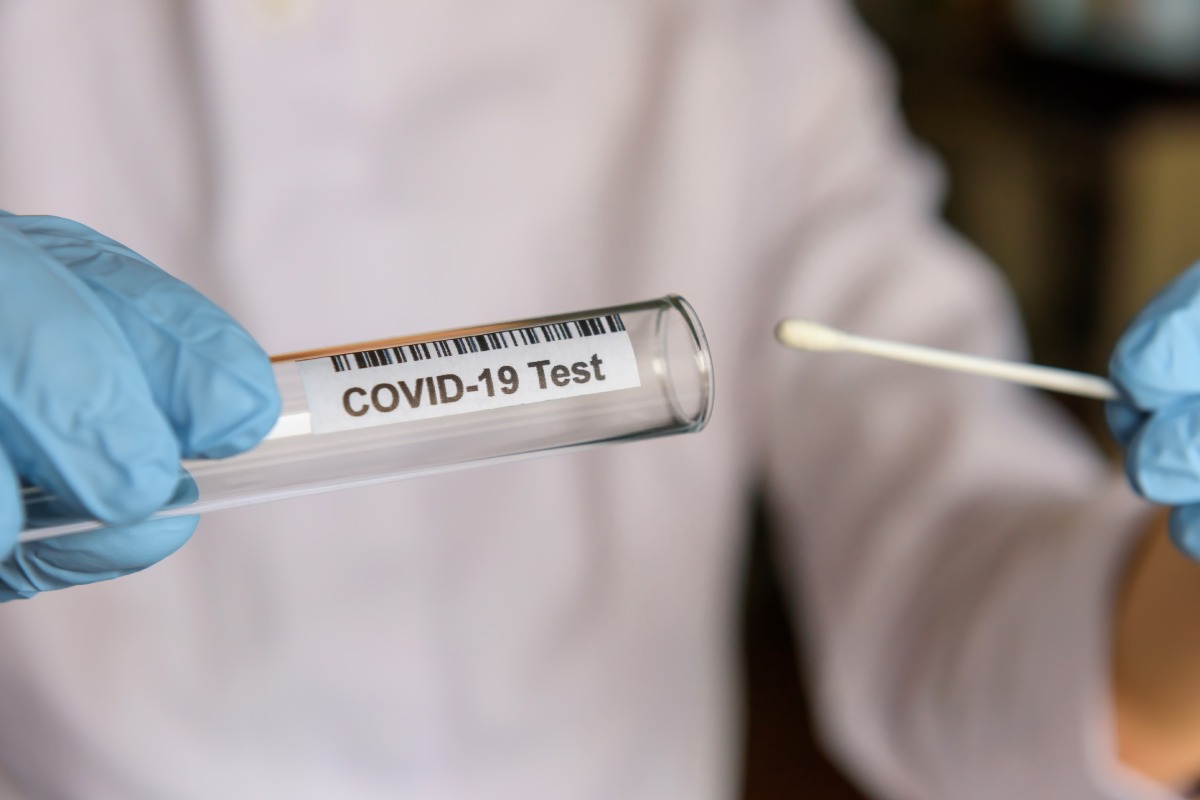 Las cifras actualizadas este jueves por el Ministerio de Sanidad arrojan 9.658 casos confirmados más.
Las cifras actualizadas este jueves por el Ministerio de Sanidad arrojan 9.658 casos confirmados más.
 El mercado farmacéutico ha aumentado un 1,4% en valores y ha decrecido un 0,5% en unidades en los últimos 12 meses.
El mercado farmacéutico ha aumentado un 1,4% en valores y ha decrecido un 0,5% en unidades en los últimos 12 meses.
 Recogida de ninos del colegio en el ultimo dia de clase despues de decretarse el cierre de centros escolares y universidades durante 15 dias por la epidemia de coronavirus. En la imagen, recogida en un colegio de Soto del Real.
Recogida de ninos del colegio en el ultimo dia de clase despues de decretarse el cierre de centros escolares y universidades durante 15 dias por la epidemia de coronavirus. En la imagen, recogida en un colegio de Soto del Real.
 Raquel Yotti, directora del ISCIII.
Raquel Yotti, directora del ISCIII.
 José Sánchez Gámez, secretario general de Satse en AndalucÃa.
José Sánchez Gámez, secretario general de Satse en AndalucÃa.
 2.640 residentes de la Comunidad Valenciana se encuentran en una protesta indefinida desde el pasado 21 de julio.
2.640 residentes de la Comunidad Valenciana se encuentran en una protesta indefinida desde el pasado 21 de julio.
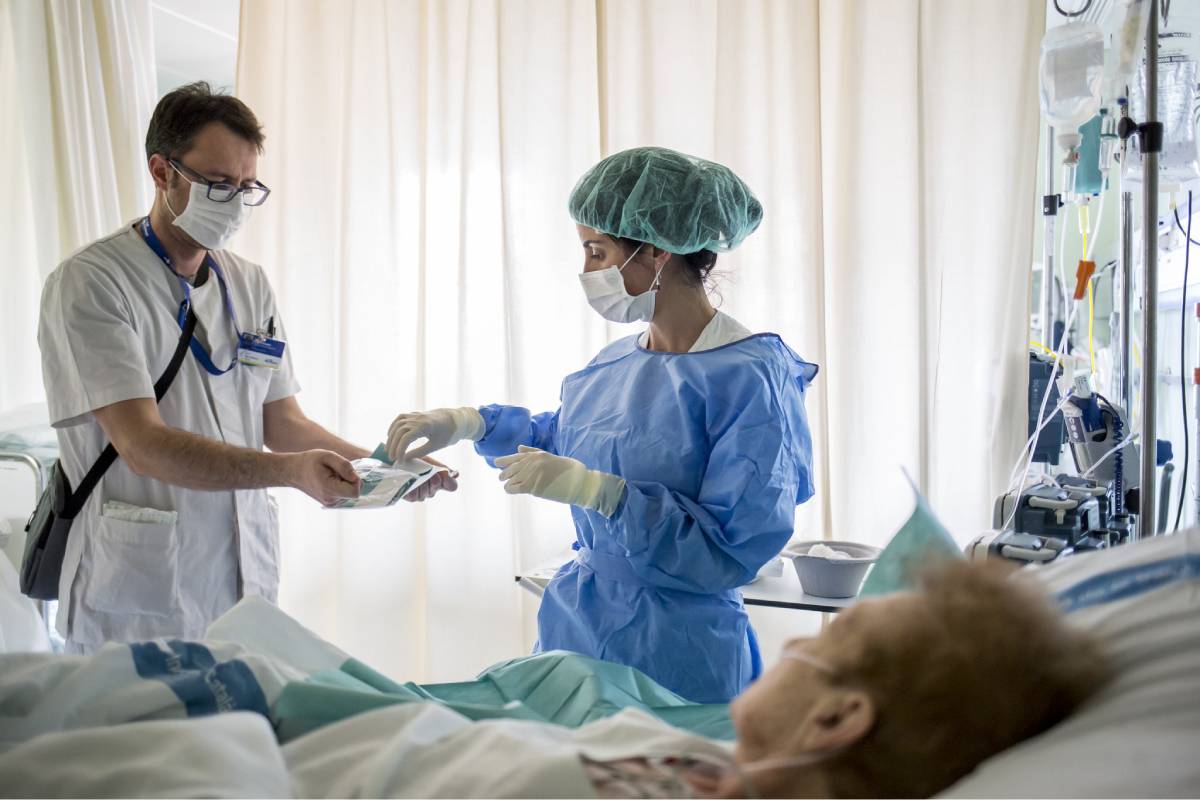 Los protocolos de atención durante la pandemia deben evaluarse.
Los protocolos de atención durante la pandemia deben evaluarse.
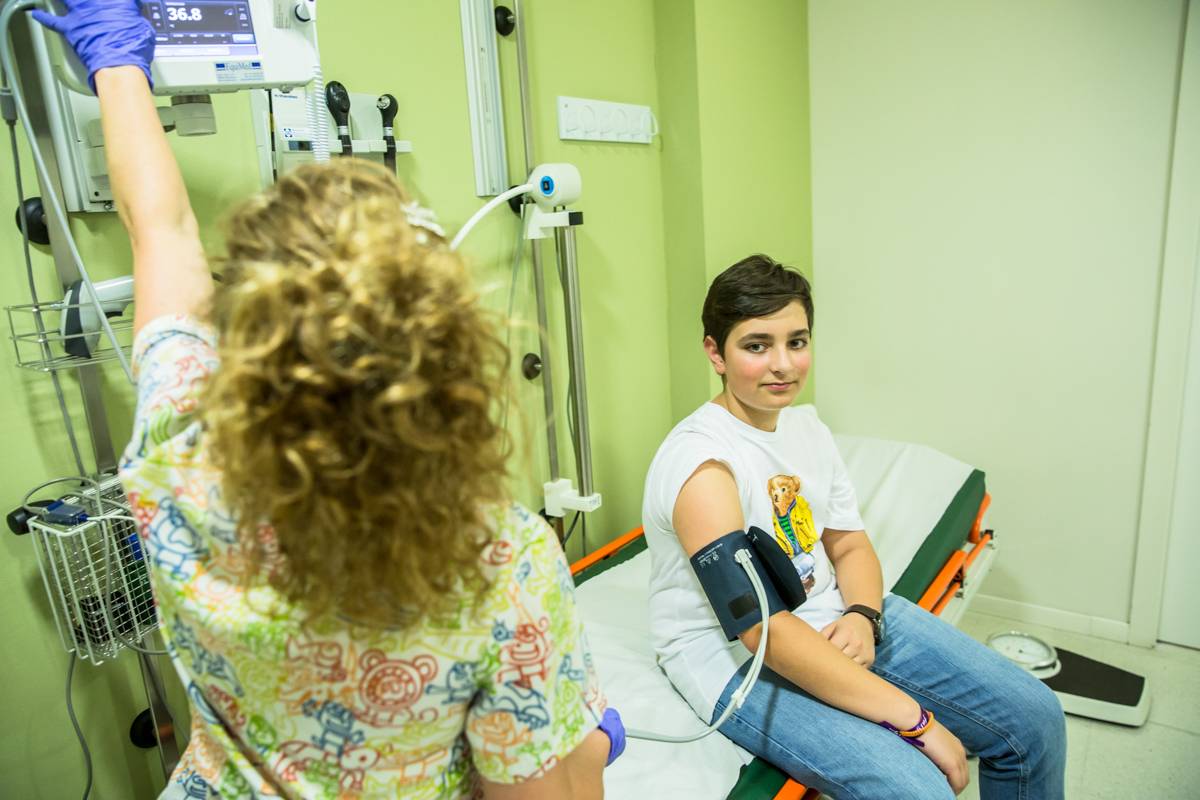 La AEEP reivindica la existencia y dotación de enfermas escolares con formación de especialista en EnfermerÃa Pediátrica. FOTO: Ariadna Creus y Ãngel GarcÃa (Banc Imatges Infermeres).
La AEEP reivindica la existencia y dotación de enfermas escolares con formación de especialista en EnfermerÃa Pediátrica. FOTO: Ariadna Creus y Ãngel GarcÃa (Banc Imatges Infermeres).
 Isabel Morales Gil, presidenta de la AEEP.
Isabel Morales Gil, presidenta de la AEEP.
 ValentÃn Fuster, director del Centro Nacional de Investigaciones Cardiovasculares (CNIC) y del Instituto Mount Sinai Heart de Nueva York.
ValentÃn Fuster, director del Centro Nacional de Investigaciones Cardiovasculares (CNIC) y del Instituto Mount Sinai Heart de Nueva York.
 Ya son 419.849 las personas que han resultado infectadas por el virus en España desde el inicio de la pandemia.
Ya son 419.849 las personas que han resultado infectadas por el virus en España desde el inicio de la pandemia.





 Salvador Illa, ministro de Sanidad.
Salvador Illa, ministro de Sanidad.
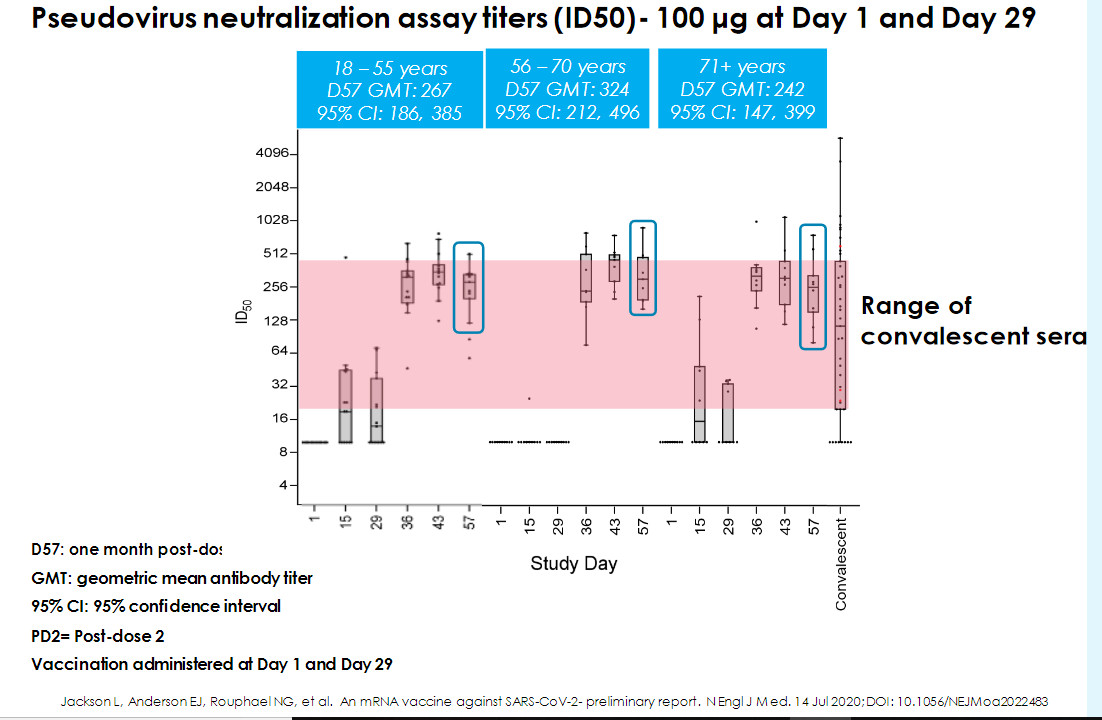
 La información previa de la compañÃa mostraba que la vacuna genera respuesta inmune relevante en voluntarios jóvenes sanos.
La información previa de la compañÃa mostraba que la vacuna genera respuesta inmune relevante en voluntarios jóvenes sanos.
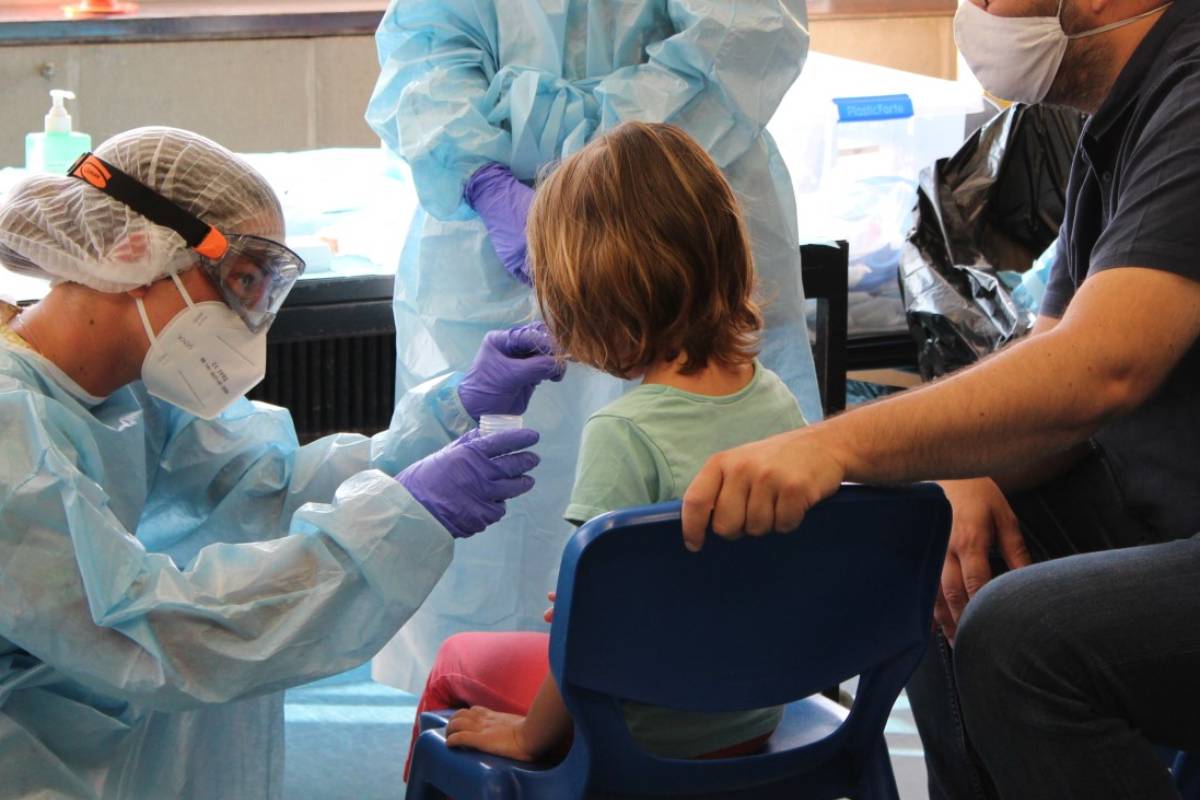
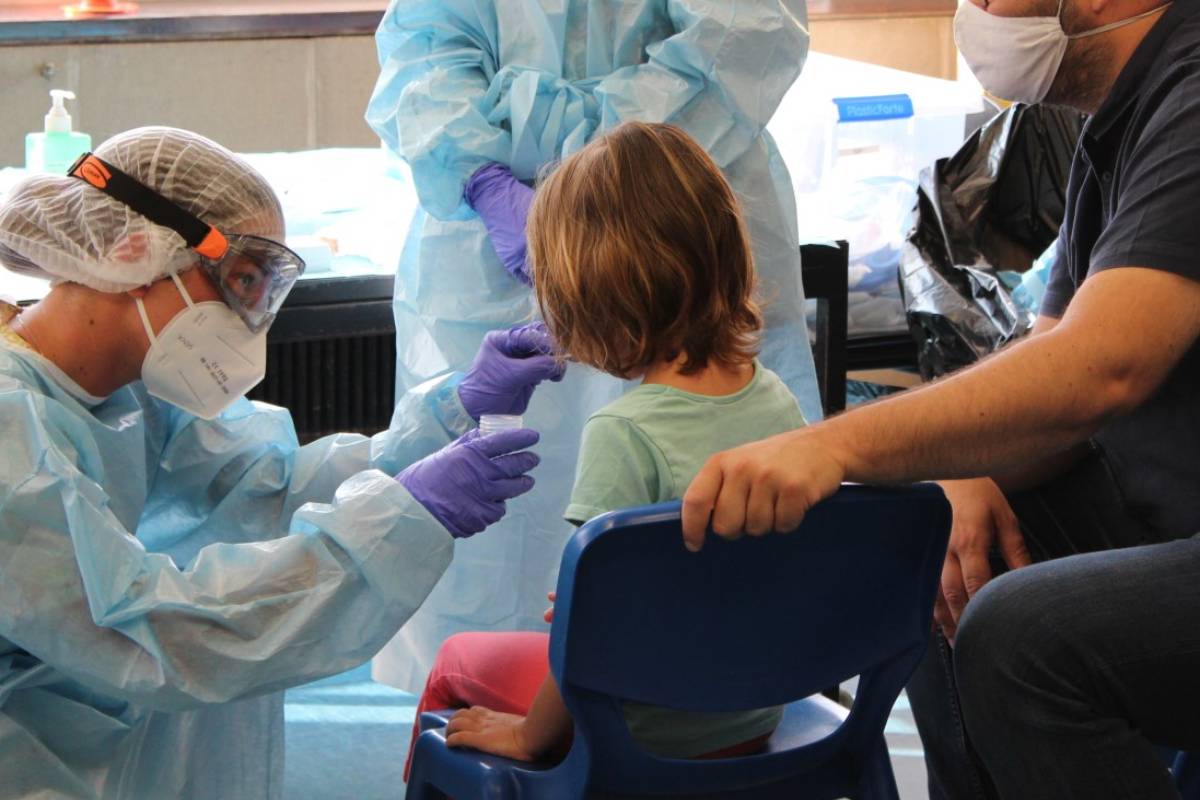 Toma de muestras para realizar pruebas de detección del Covid-19 a un niño.(Foto: Sant Joan de Déu).
Toma de muestras para realizar pruebas de detección del Covid-19 a un niño.(Foto: Sant Joan de Déu).
 Centro de salud de Madrid durante la epidemia de coronavirus (José Luis Pindado)
Centro de salud de Madrid durante la epidemia de coronavirus (José Luis Pindado)
 Marina Pollán, directora del Centro de EpidemiologÃa del Instituto de Salud Carlos III.
Marina Pollán, directora del Centro de EpidemiologÃa del Instituto de Salud Carlos III.
 El ensayo español Épicos se extiende a Latinoamérica.
El ensayo español Épicos se extiende a Latinoamérica.
 Intervención del ministro de Sanidad, Salvador Illa, en los cursos de verano de la UIMP.
Intervención del ministro de Sanidad, Salvador Illa, en los cursos de verano de la UIMP.


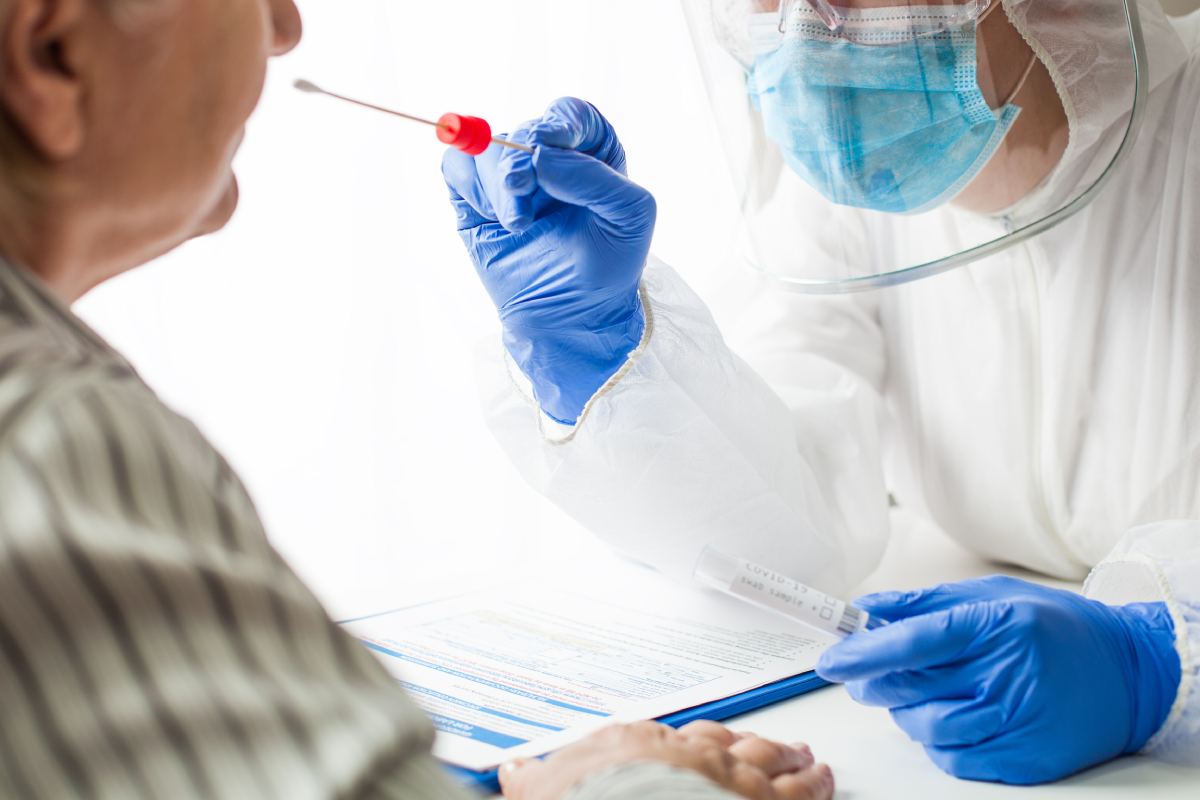







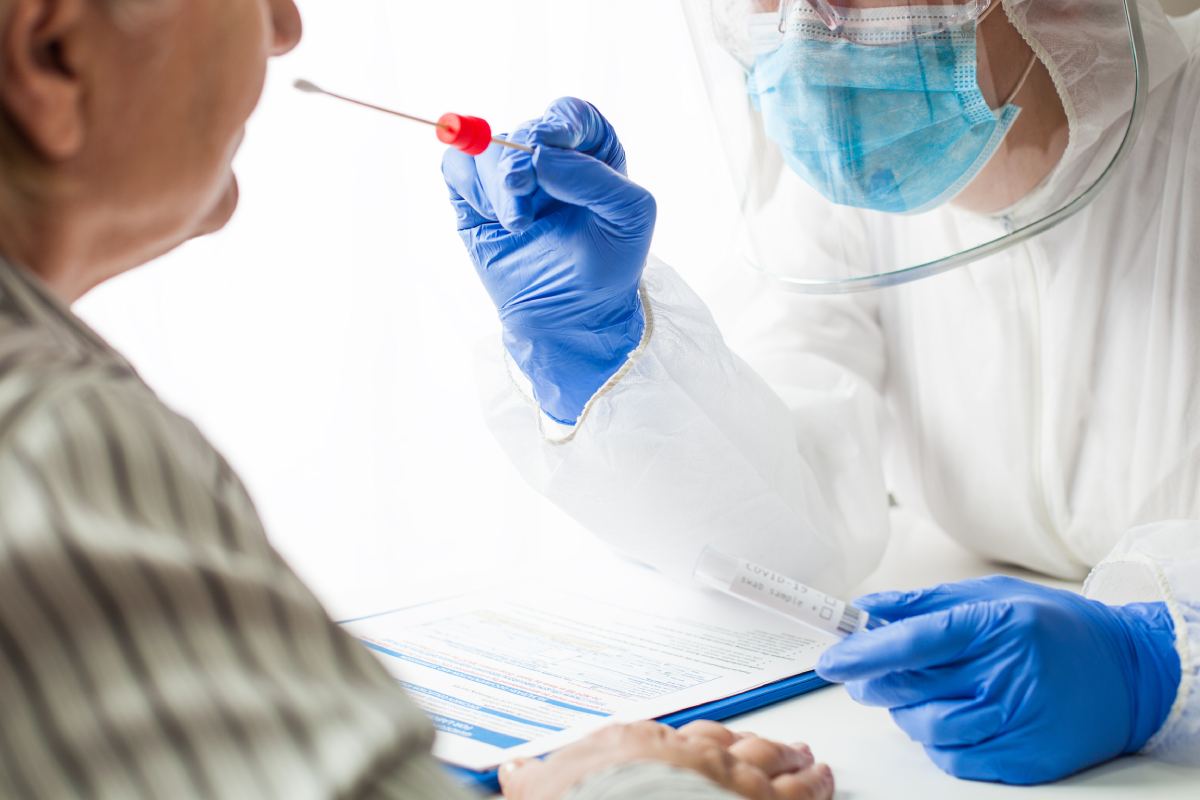 Las cifras actualizadas y difundidas este martes por el Ministerio de Sanidad registran 7.117 nuevos casos desde ayer.
Las cifras actualizadas y difundidas este martes por el Ministerio de Sanidad registran 7.117 nuevos casos desde ayer.
 El uso de mascarillas está siendo obligatorio en varias comunidades autónomas,aunque se mantenga el distanciamiento social.
El uso de mascarillas está siendo obligatorio en varias comunidades autónomas,aunque se mantenga el distanciamiento social.
 Pedro Sánchez, presidente del Gobierno.
Pedro Sánchez, presidente del Gobierno.
 Prueba PCR durante un cribado organizado por Osakidetza (EFE/Javier Etxezarreta)
Prueba PCR durante un cribado organizado por Osakidetza (EFE/Javier Etxezarreta)
 Señalan que el 15% de los pacientes Covid-19 hospitalizados desarrollan trombosis venosas asintomáticas.
Señalan que el 15% de los pacientes Covid-19 hospitalizados desarrollan trombosis venosas asintomáticas.
 Reunión del Comité asesor externo para el balance de la gestión de la pandemia Covid-19 de AndalucÃa.
Reunión del Comité asesor externo para el balance de la gestión de la pandemia Covid-19 de AndalucÃa.
 Los farmacéuticos proponen tener una mayor implicación en la 'vuelta al cole' para contribuir a que sea lo más segura posible.
Los farmacéuticos proponen tener una mayor implicación en la 'vuelta al cole' para contribuir a que sea lo más segura posible.
 El autor sostiene que vivimos en la era de la explosión de los algoritmos de aprendizaje automático, basados en la imitación de las redes neuronales humanas.
El autor sostiene que vivimos en la era de la explosión de los algoritmos de aprendizaje automático, basados en la imitación de las redes neuronales humanas.
 SerafÃn Romero, presidente de la Organización Médica Colegial (OMC) (Mauricio Skrycky)
SerafÃn Romero, presidente de la Organización Médica Colegial (OMC) (Mauricio Skrycky)
 El director del Centro de Coordinación de Alertas y Emergencias Sanitarias, Fernando Simón, comparece en rueda de prensa para dar cuenta de los últimos datos de la pandemia de coronavirus en España, este lunes en la sede del Ministerio de Sanidad, en Madrid (EFE/Rodrigo Jiménez)
El director del Centro de Coordinación de Alertas y Emergencias Sanitarias, Fernando Simón, comparece en rueda de prensa para dar cuenta de los últimos datos de la pandemia de coronavirus en España, este lunes en la sede del Ministerio de Sanidad, en Madrid (EFE/Rodrigo Jiménez)
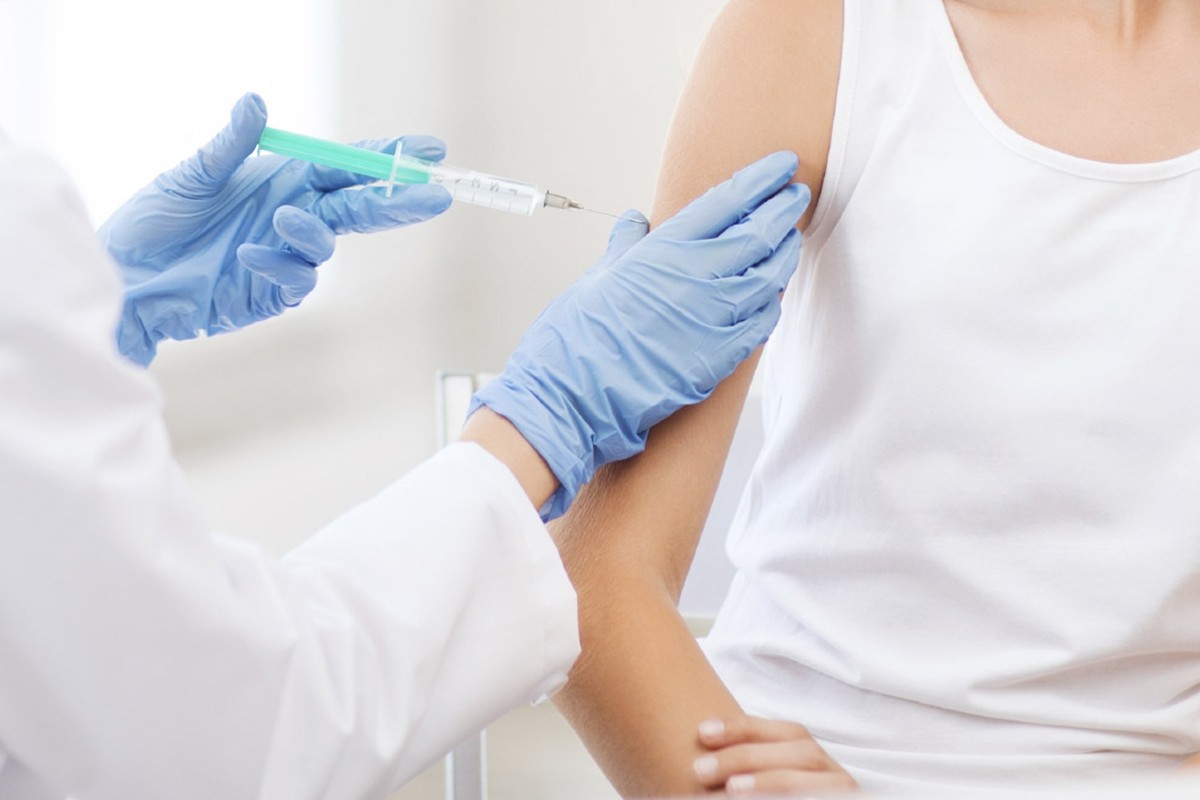






 Moderna ha incrementado su fabricación mundial con el objetivo de suministrar aproximadamente 500 millones de dosis al año con la posibilidad de alcanzar 1.000 millones, a partir de 2021.
Moderna ha incrementado su fabricación mundial con el objetivo de suministrar aproximadamente 500 millones de dosis al año con la posibilidad de alcanzar 1.000 millones, a partir de 2021.
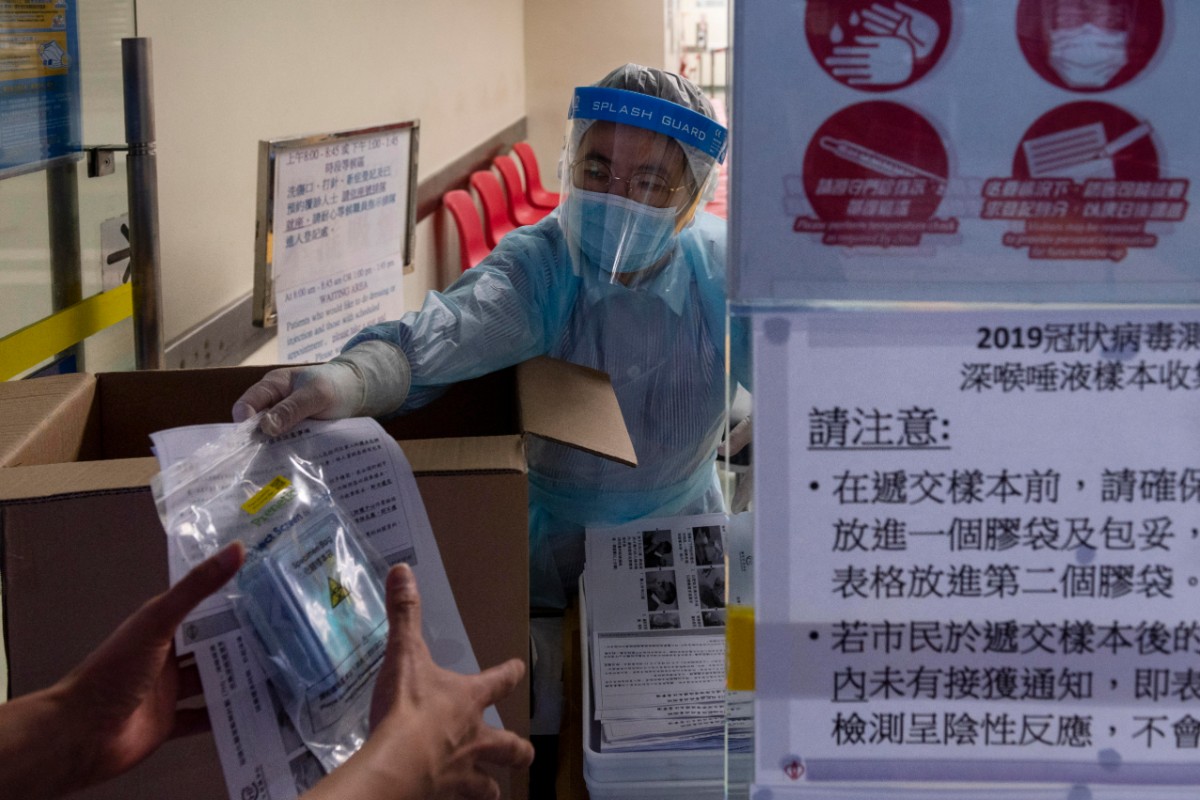
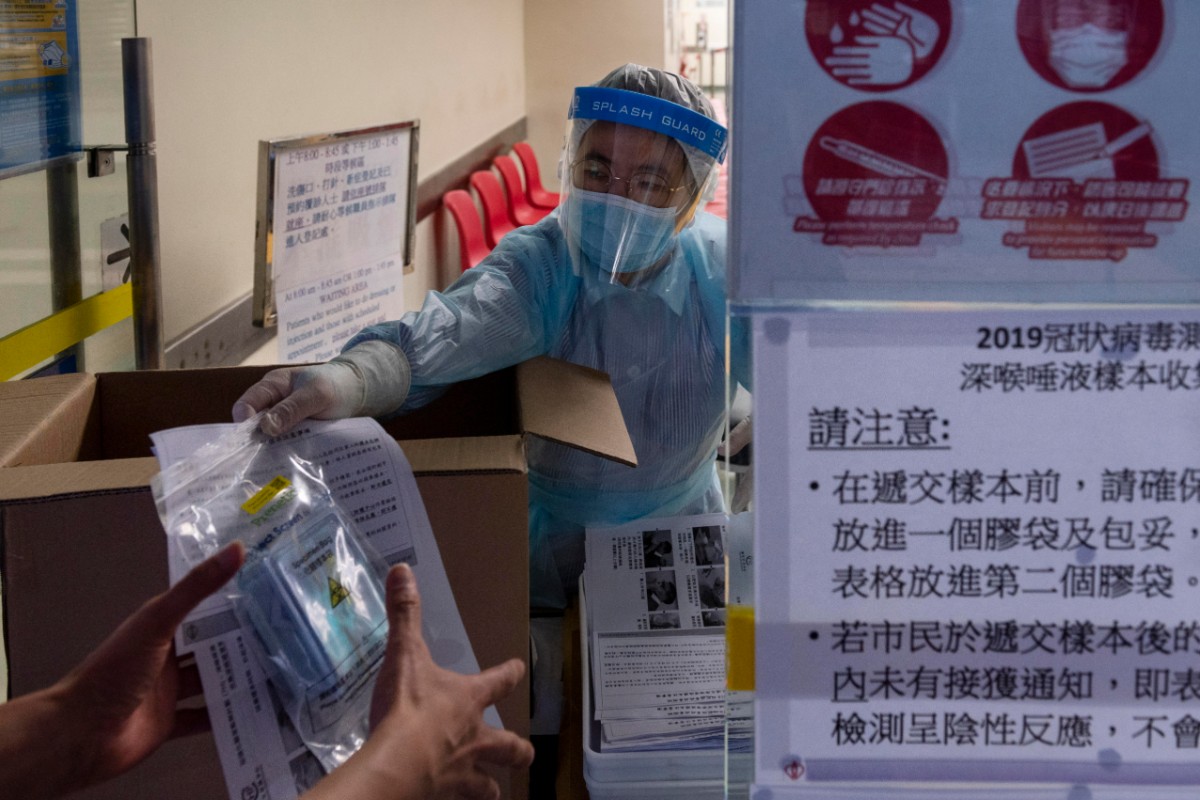 Reparto de test de Covid-19 en Hong Kong (EFE/EPA/Miguel Candela)
Reparto de test de Covid-19 en Hong Kong (EFE/EPA/Miguel Candela)
 Torra ha explicado que la prohibición de las reuniones sociales se debe a que un 70% de los contagios que se están diagnosticando se originan en reuniones sociales, familiares o con amigos.
Torra ha explicado que la prohibición de las reuniones sociales se debe a que un 70% de los contagios que se están diagnosticando se originan en reuniones sociales, familiares o con amigos.
 Un portavoz del Comité de Huelga MIR de la Comunidad Valenciana hablando en un encuentro informal con la consejera de Sanidad, Ana Barceló, durante una visita de ésta al Hospital de Alicante (Fotos: Huelga MIR CV)
Un portavoz del Comité de Huelga MIR de la Comunidad Valenciana hablando en un encuentro informal con la consejera de Sanidad, Ana Barceló, durante una visita de ésta al Hospital de Alicante (Fotos: Huelga MIR CV)
 El Consejero de Sanidad de Murcia, Manuel Villegas (EFE/Marcial Guillén)
El Consejero de Sanidad de Murcia, Manuel Villegas (EFE/Marcial Guillén)
 La autorización está respaldada por los resultados de dos estudios internacionales de fase 3 que mostraron mejorÃas estadÃstica y clÃnicamente significativas en la función pulmonar.
La autorización está respaldada por los resultados de dos estudios internacionales de fase 3 que mostraron mejorÃas estadÃstica y clÃnicamente significativas en la función pulmonar.
 Enfermera del Hospital Sant Joan de Déu ayuda a un joven a utilizar un inhalador con un dispositivo espaciador. FOTO: Ariadna Creus y Ãngel GarcÃa.
Enfermera del Hospital Sant Joan de Déu ayuda a un joven a utilizar un inhalador con un dispositivo espaciador. FOTO: Ariadna Creus y Ãngel GarcÃa.
 Los médicos piden tomar medidas para controlar los contagios de Covid-19 antes de que se vuelva a desbordar la capacidad del sistema (José Luis Pindado)
Los médicos piden tomar medidas para controlar los contagios de Covid-19 antes de que se vuelva a desbordar la capacidad del sistema (José Luis Pindado)





 De los primeros 90 voluntarios de la vacuna italiana, la mitad tiene entre 18 y 55 años y la otra entre 65 y 85 años.
De los primeros 90 voluntarios de la vacuna italiana, la mitad tiene entre 18 y 55 años y la otra entre 65 y 85 años.
 Aspecto de la sala de espera en la consulta de un centro de salud.
Aspecto de la sala de espera en la consulta de un centro de salud.
 Familia fue, de hecho, la especialidad que más se benefició del incremento adicional de puestos de formación sanitaria especializada acordado por la Comisión de Recursos Humanos del Sistema Nacional de Salud (SNS) el pasado 5 de mayo, en virtud de las necesidades de efectivos a corto y medio plazo que se preveÃan en algunas especialidades para afrontar las consecuencias de la crisis sanitaria generada por la Covid-19. Pese a todo, la especialidad de primaria agotó este año todas su plazas, bien es verdad que en la decimoquinta y última jornada de adjudicación.
Familia fue, de hecho, la especialidad que más se benefició del incremento adicional de puestos de formación sanitaria especializada acordado por la Comisión de Recursos Humanos del Sistema Nacional de Salud (SNS) el pasado 5 de mayo, en virtud de las necesidades de efectivos a corto y medio plazo que se preveÃan en algunas especialidades para afrontar las consecuencias de la crisis sanitaria generada por la Covid-19. Pese a todo, la especialidad de primaria agotó este año todas su plazas, bien es verdad que en la decimoquinta y última jornada de adjudicación. La condición fÃsica influye en la conectividad funcional del hipocampo de los niños
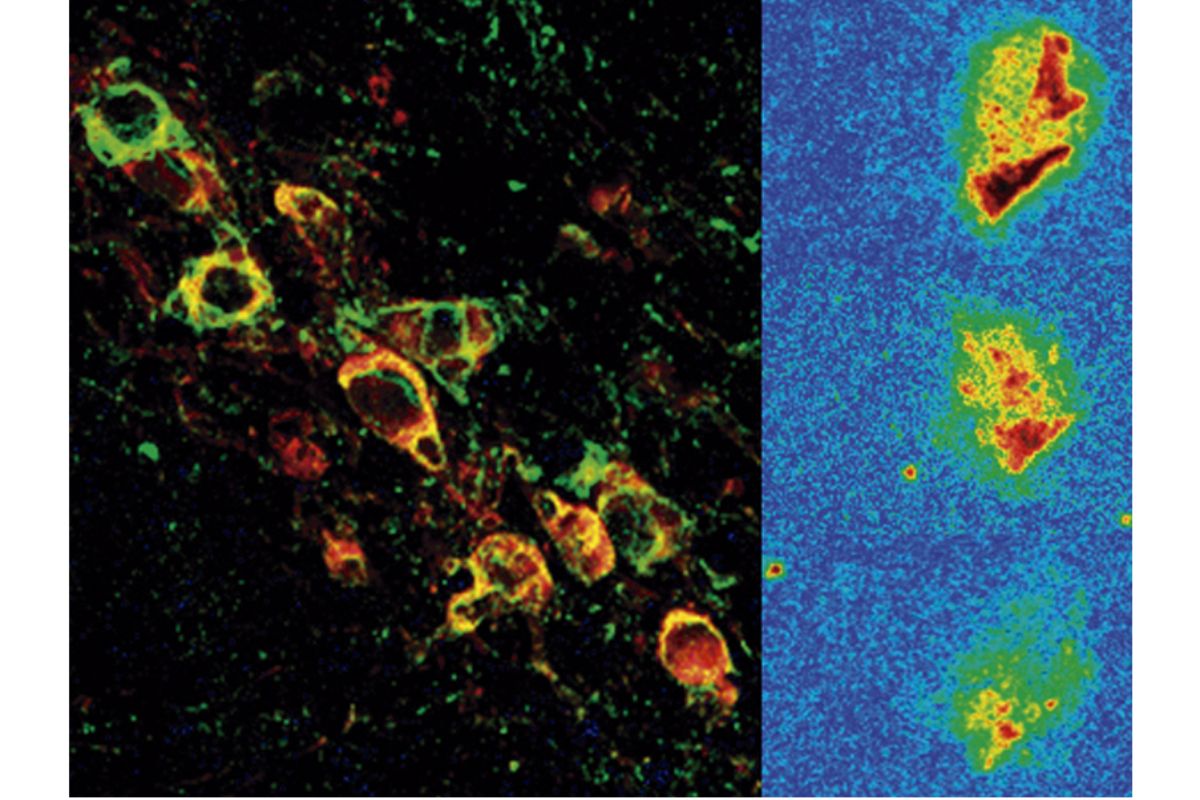
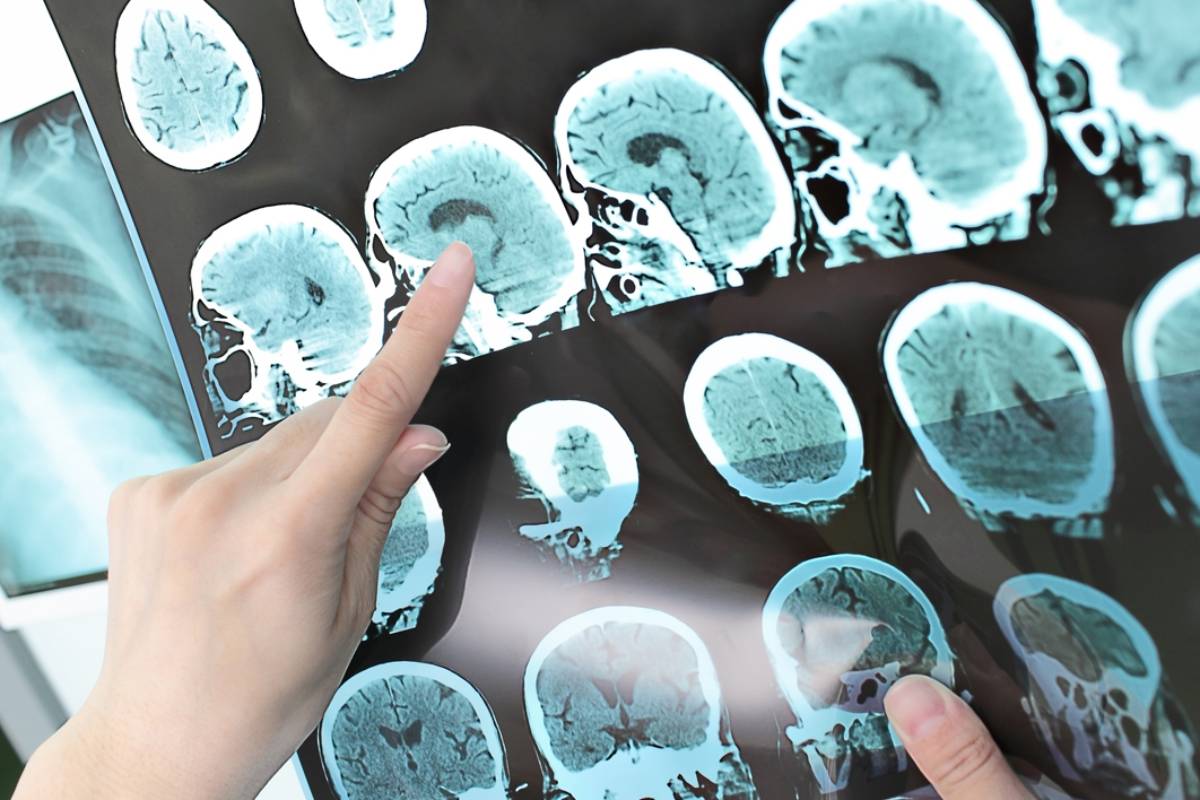
La condición fÃsica influye en la conectividad funcional del hipocampo de los niños
 El preservativo  es un artÃculo que parece que se le está escapando de las manos a la farmacia y que, sin embargo, está creciendo en grandes superficies.
El preservativo  es un artÃculo que parece que se le está escapando de las manos a la farmacia y que, sin embargo, está creciendo en grandes superficies.
 Campaña sobre Salud sexual en Farmacia Boix (Valencia).
Campaña sobre Salud sexual en Farmacia Boix (Valencia).
 sofocos
sofocos
 La Novena SinfonÃa de Ludwig van Beethoven se ha utilizado en un estudio para demostrar la existencia de las 'células conceptuales'.
La Novena SinfonÃa de Ludwig van Beethoven se ha utilizado en un estudio para demostrar la existencia de las 'células conceptuales'.
 El profesor del MIT Jerry Lettvin acuñó el término de "célula de la abuela".
El profesor del MIT Jerry Lettvin acuñó el término de "célula de la abuela".










 Sanitario atendiendo a un paciente ingresado en una UCI
Sanitario atendiendo a un paciente ingresado en una UCI
 Según los neonatólogos, los bebés de madres con Covid-19 han nacido sanos, aunque los contagios se produjeron en el tercer trimestre
Según los neonatólogos, los bebés de madres con Covid-19 han nacido sanos, aunque los contagios se produjeron en el tercer trimestre
 Logotipo de la AELIP (Asociación de Familiares y Afectados de Lipodistrofias).
Logotipo de la AELIP (Asociación de Familiares y Afectados de Lipodistrofias).

 Se necesitan buenos cursos para aprender a investigar
Se necesitan buenos cursos para aprender a investigar
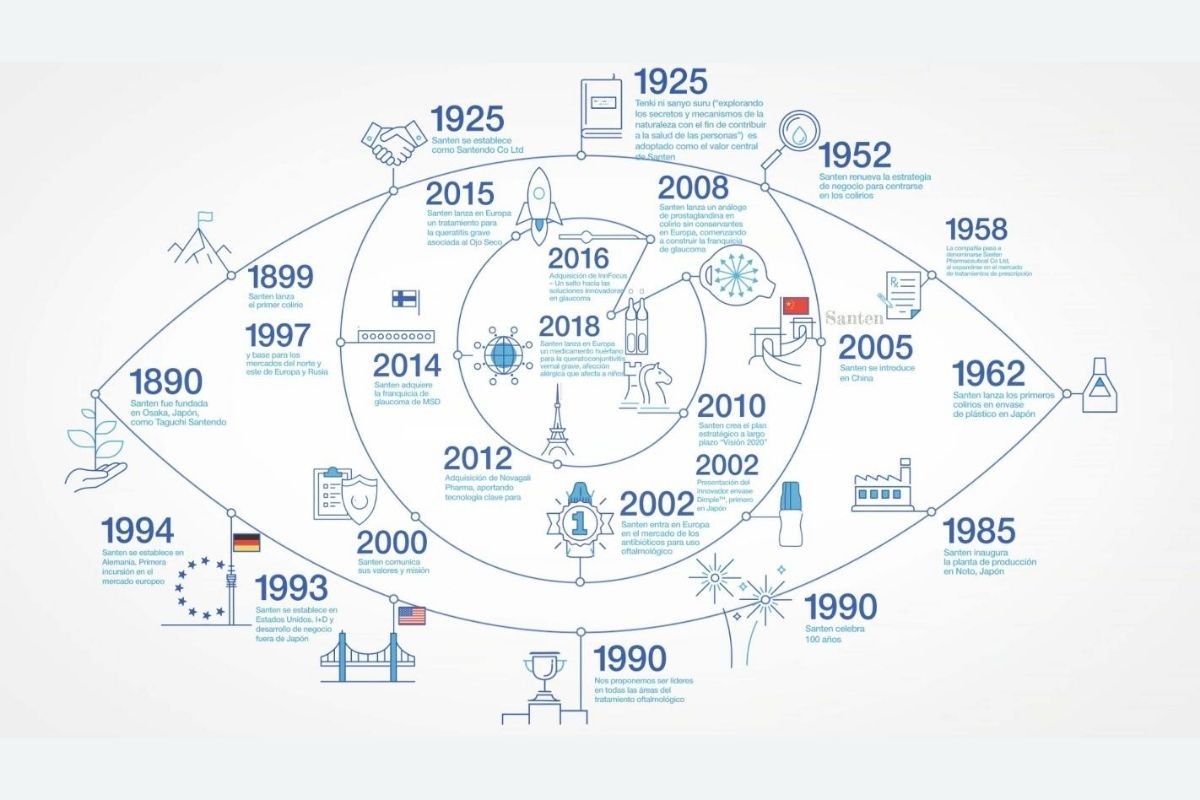
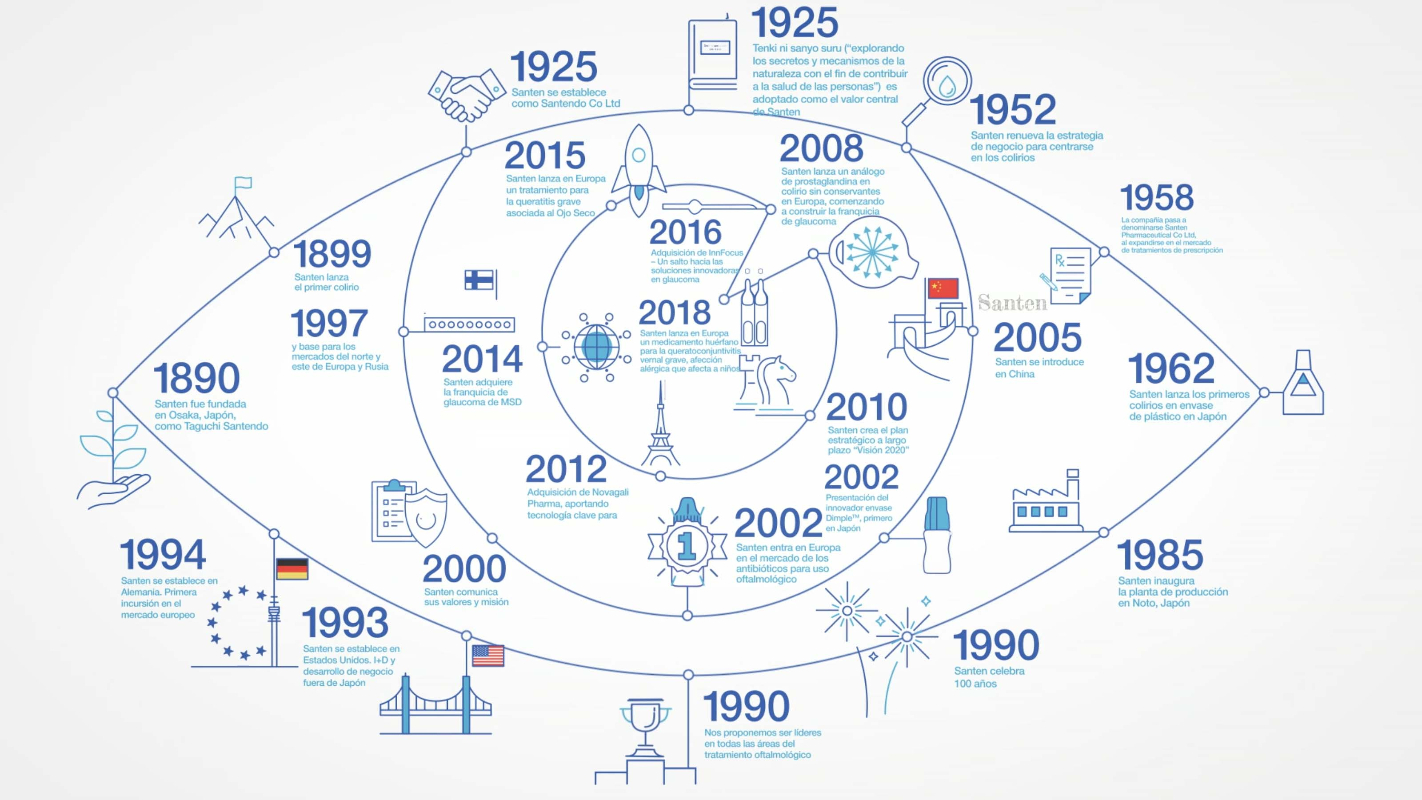
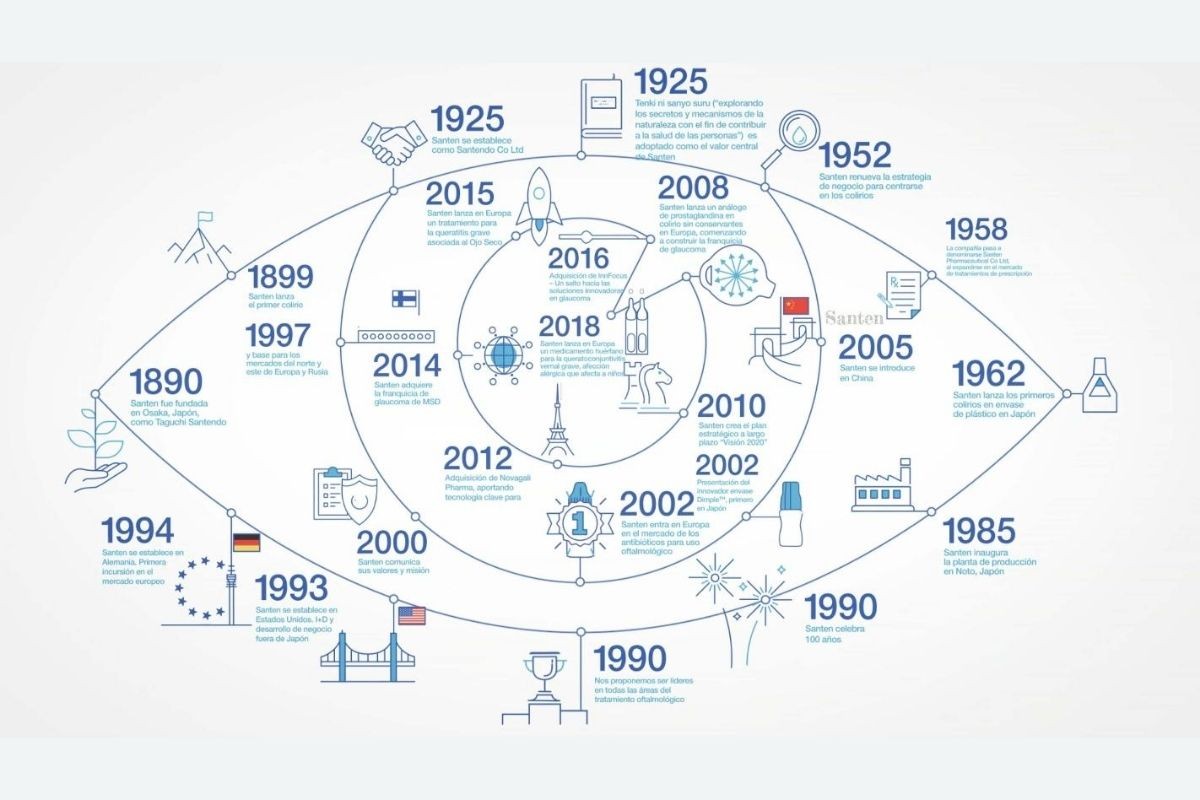 La compañÃa de origen japonés acaba de celebrar su 130 aniversario.
La compañÃa de origen japonés acaba de celebrar su 130 aniversario.
 VÃctor González Monje hace balance de los 5 años de presencia de la compañÃa en España.
VÃctor González Monje hace balance de los 5 años de presencia de la compañÃa en España.
 El apoyo y el respaldo de los compañeros son de gran ayuda para eliminar miedos en los primeros dÃas de residencia.
El apoyo y el respaldo de los compañeros son de gran ayuda para eliminar miedos en los primeros dÃas de residencia.
 Grupo multidisciplinar de rastreadores en Logroño (EFE/Raquel Manzanares)
Grupo multidisciplinar de rastreadores en Logroño (EFE/Raquel Manzanares)
 José Ramón MartÃnez Riera, presidente de la Asociación de EnfermerÃa Comunitaria (AEC).
José Ramón MartÃnez Riera, presidente de la Asociación de EnfermerÃa Comunitaria (AEC).
 El consumo crónico del cannabis transforma el carácter en muchas personas.
El consumo crónico del cannabis transforma el carácter en muchas personas.
 Un hassasin acaba con la vida del estadista Nizam al Mulk.
Un hassasin acaba con la vida del estadista Nizam al Mulk.
 La Comisión Europea emitió el 3 de julio una autorización de comercialización condicional para remdesivir en Covid-19.
La Comisión Europea emitió el 3 de julio una autorización de comercialización condicional para remdesivir en Covid-19.
 Un voluntario de MSF acompaña a una anciana en una residencia (Olmo Calvo/MSF)
Un voluntario de MSF acompaña a una anciana en una residencia (Olmo Calvo/MSF)
 Una médico muestra un test de Covid realizado en un centro de salud de Brión, La Coruña (Foto: EFE).
Una médico muestra un test de Covid realizado en un centro de salud de Brión, La Coruña (Foto: EFE).











 Ofatumumab ha sido autorizado como ‘Kesimpta’ en formas recurrentes de esclerosis múltiple.
Ofatumumab ha sido autorizado como ‘Kesimpta’ en formas recurrentes de esclerosis múltiple.
 Ricardo Gómez Huelgas, presidente de la Sociedad Española de Medicina Interna (SEMI)
Ricardo Gómez Huelgas, presidente de la Sociedad Española de Medicina Interna (SEMI)
 Según el acuerdo, Roche se encargarÃa de los trámites de autorización con la EMA.
Según el acuerdo, Roche se encargarÃa de los trámites de autorización con la EMA.
 Un hombre fumando tras bajarse la mascarilla. (EFE/Fernando Alvarado)
Un hombre fumando tras bajarse la mascarilla. (EFE/Fernando Alvarado)
 Farmacia rural.
Farmacia rural.
 Un sanitario toma la temperatura a un hombre antes de acceder al Centro de Salud de Los Ãngeles, en el distrito de Villaverde, donde el gobierno regional ha puesto en marcha uno de los dispositivos de pruebas PCR para tratar de detectar asintomáticos de 15 a 49 años en las áreas de la región con mayor incidencia de COVID-19. (EFE/Mariscal)
Un sanitario toma la temperatura a un hombre antes de acceder al Centro de Salud de Los Ãngeles, en el distrito de Villaverde, donde el gobierno regional ha puesto en marcha uno de los dispositivos de pruebas PCR para tratar de detectar asintomáticos de 15 a 49 años en las áreas de la región con mayor incidencia de COVID-19. (EFE/Mariscal)
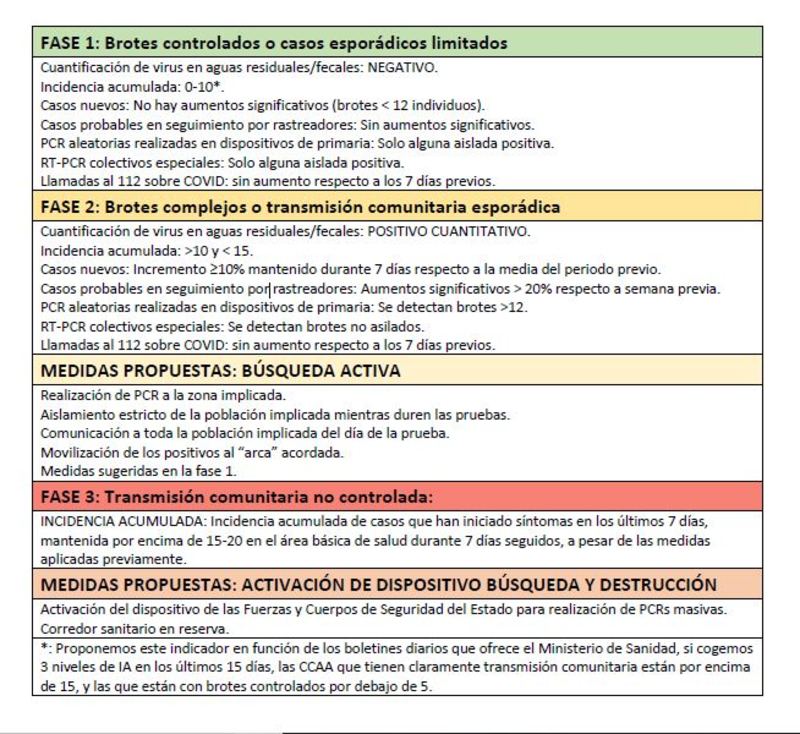 Medidas contempladas en las distintas fases recogidas en el documento de consenso.
Medidas contempladas en las distintas fases recogidas en el documento de consenso.





 Fernando Simón, director del Centro de Alertas y Emergencias Sanitarias del Ministerio de Sanidad. (EFE)
Fernando Simón, director del Centro de Alertas y Emergencias Sanitarias del Ministerio de Sanidad. (EFE)
 Christopher Hansung Ko, presidente y director ejecutivo de Samsung Bioepis
Christopher Hansung Ko, presidente y director ejecutivo de Samsung Bioepis
 El Gobierno señala que ningún usuario puede ser identificado o localizado mediante la app.
El Gobierno señala que ningún usuario puede ser identificado o localizado mediante la app.